¿Qué es GxP y por qué es importante en las industrias farmacéutica y biotecnológica?
GxP es un término clave que engloba las normativas y buenas prácticas esenciales en sectores como el farmacéutico, biotecnológico y de dispositivos médicos. La “x” en GxP se refiere a áreas específicas de aplicación, como:
- GMP (Buenas Prácticas de Fabricación): Asegura procesos de fabricación seguros y controlados.
- GDP (Buenas Prácticas de Distribución): Garantiza la correcta gestión en la cadena de suministro.
- GLP (Buenas Prácticas de Laboratorio): Establece normas para generar datos confiables en investigación.
- GCP (Buenas Prácticas Clínicas): Protege a los participantes en ensayos clínicos y asegura la validez de los resultados.
Estas normativas son fundamentales para garantizar la calidad, seguridad y eficacia de los productos farmacéuticos, desde la investigación inicial hasta su distribución. Cumplir con GxP no solo asegura la confianza del consumidor, sino que también cumple con requisitos regulatorios globales.

Buenas Prácticas de Fabricación (GMP)

Las GMP se basan en las directrices de la Administración de Alimentos y Medicamentos de EE. UU. (FDA) y regulan la fabricación de productos farmacéuticos y otros productos médicos para garantizar que se produzcan de forma coherente de acuerdo con estrictos estándares de calidad. Estas prácticas tienen como objetivo evitar la contaminación, errores de fabricación u otros problemas que puedan afectar a la calidad del producto final.
Las buenas prácticas de fabricación son aplicadas por agencias reguladoras de todo el mundo, como la FDA (Administración de Alimentos y Medicamentos), la EMA (Agencia Europea de Medicamentos) y la OMS (Organización Mundial de la Salud).
Elementos clave de las GMP:
- Control de la calidad: Cada etapa de la fabricación de la industria farmacéutica debe ser monitoreada con pruebas e inspecciones periódicas de las materias primas, productos intermedios y productos terminados.
- Validación de procesos: Los procesos de producción, limpieza y mantenimiento deben validarse para garantizar que el producto cumpla con las especificaciones requeridas.
- Formación del personal: Todo el personal involucrado en la producción debe estar adecuadamente formado en procedimientos y estándares de calidad.
- Trazabilidad: Las buenas prácticas de fabricación requieren una documentación completa y precisa para rastrear cada lote de producción, lo que permite seguir un historial completo de fabricación y distribución en caso de que surja algún problema.
Buenas Prácticas de Distribución (GDP)
Las GDP se centran en la distribución de productos farmacéuticos. El objetivo de las GDP es prevenir el deterioro del producto, minimizar el riesgo de falsificación y garantizar que los medicamentos se transporten y almacenen en condiciones adecuadas.
Elementos clave de las GDP:
- Almacenamiento y transporte: Los productos deben almacenarse en condiciones estrictamente controladas de temperatura y humedad. Se recomienda, por ejemplo, contar con sistemas de monitoreo y mapeo de las áreas de almacenamiento para garantizar el cumplimiento de los estándares establecidos.
- Trazabilidad: Cada lote de medicamento o producto farmacéutico debe ser rastreable desde la fabricación hasta la entrega al paciente, lo que permite una fácil retirada y garantiza que ningún producto falsificado entre en la cadena de suministro legítima.
- Formación y cualificación del personal: Los distribuidores deben asegurarse de que el personal en cada etapa de la distribución esté debidamente formado para manejar los productos y cumplir con los procedimientos de las GDP.
- Quejas y retiradas del mercado: Deben existir procedimientos para abordar las quejas y organizar retiradas puntuales y precisas si es necesario.

Buenas Prácticas de Laboratorio (GLP)

Las GLP rigen los estudios de seguridad no clínicos para productos farmacéuticos y otros productos regulados. Estas directrices garantizan que los datos de laboratorio sean fiables, verificables y reproducibles, lo que permite utilizar con confianza los resultados de los estudios en las solicitudes de autorización de comercialización.
Elementos clave de las GLP:
- Organización del estudio: Las GLP requieren una definición clara de las funciones y responsabilidades de cada miembro del equipo de investigación, junto con un plan de estudio detallado.
- Documentación: Todas las actividades y observaciones deben registrarse en tiempo real y documentarse rigurosamente para permitir la trazabilidad completa de los datos experimentales.
- Instalaciones y equipamiento: Los laboratorios deben diseñarse y mantenerse para minimizar los riesgos de contaminación. Todos los equipos deben ser mantenidos y calibrados regularmente de acuerdo con procedimientos conformes para garantizar resultados fiables.
- Archivo de datos: Los datos deben almacenarse de forma segura para las auditorías de las autoridades reguladoras pertinentes.
Buenas Prácticas Clínicas (GCP)
Las GCP se aplican a los ensayos clínicos realizados en seres humanos, lo que garantiza los derechos, la seguridad y el bienestar de los participantes, al tiempo que garantiza que los datos recopilados sean fiables y precisos. Las GCP son cruciales para los ensayos clínicos de fase I a IV que evalúan la eficacia y los efectos secundarios de un medicamento antes de su lanzamiento al mercado.
Elementos clave de las GCP:
- Consentimiento informado: Los participantes deben ser informados sobre todos los aspectos del ensayo clínico y deben dar su consentimiento libremente antes de participar.
- Protocolo del estudio: Cada ensayo clínico debe seguir un protocolo estricto aprobado por los comités de ética, en el que se detallan los objetivos del estudio, los criterios de elegibilidad y los métodos de evaluación.
- Calidad de los datos: Los datos recopilados deben ser completos y precisos. Se pueden realizar auditorías para verificar la integridad de los datos recopilados durante los ensayos.
- Seguimiento y gestión de riesgos: Los ensayos clínicos deben ser monitoreados continuamente para identificar rápidamente riesgos o incidentes que podrían afectar la seguridad de los participantes o la validez de los resultados.
Las GCP están coordinadas por organizaciones intergubernamentales como el Consejo Internacional de Armonización (ICH), que publica directrices reconocidas por la mayoría de los organismos reguladores de todo el mundo, incluidas la FDA y la EMA.

GxP en la industria farmacéutica: La importancia del monitoreo ambiental
El monitoreo continuo es un aspecto crítico de GxP para garantizar la calidad de los productos farmacéuticos a lo largo de su ciclo de vida. Dickson es un experto reconocido a nivel mundial en la fabricación, implementación y mantenimiento de soluciones de monitoreo continuo. Nuestros registradores de datos, software, soluciones de mapeo, laboratorios de calibración y procedimientos rigurosos desempeñan un papel clave para ayudar a las empresas farmacéuticas a mantener el cumplimiento de las buenas prácticas de fabricación, especialmente en lo que respecta a la temperatura, la humedad y otros parámetros críticos como el monitoreo de dióxido de carbono (CO2).
La experiencia de Dickson en el monitoreo ambiental de GxP
Dickson ofrece una amplia gama de productos y servicios diseñados para cumplir con los estrictos requisitos de las directrices GMP, GDP, GLP y GCP. Estas soluciones incluyen registradores de datos conectados, sistemas de alerta y monitoreo en tiempo real, laboratorios de calibración acreditados y software de gestión de datos, todos diseñados para brindar una precisión y fiabilidad óptimas en entornos críticos. Mediante el uso de nuestras soluciones, puede monitorear y documentar continuamente los parámetros ambientales en sus centros de producción, almacenamiento y distribución.
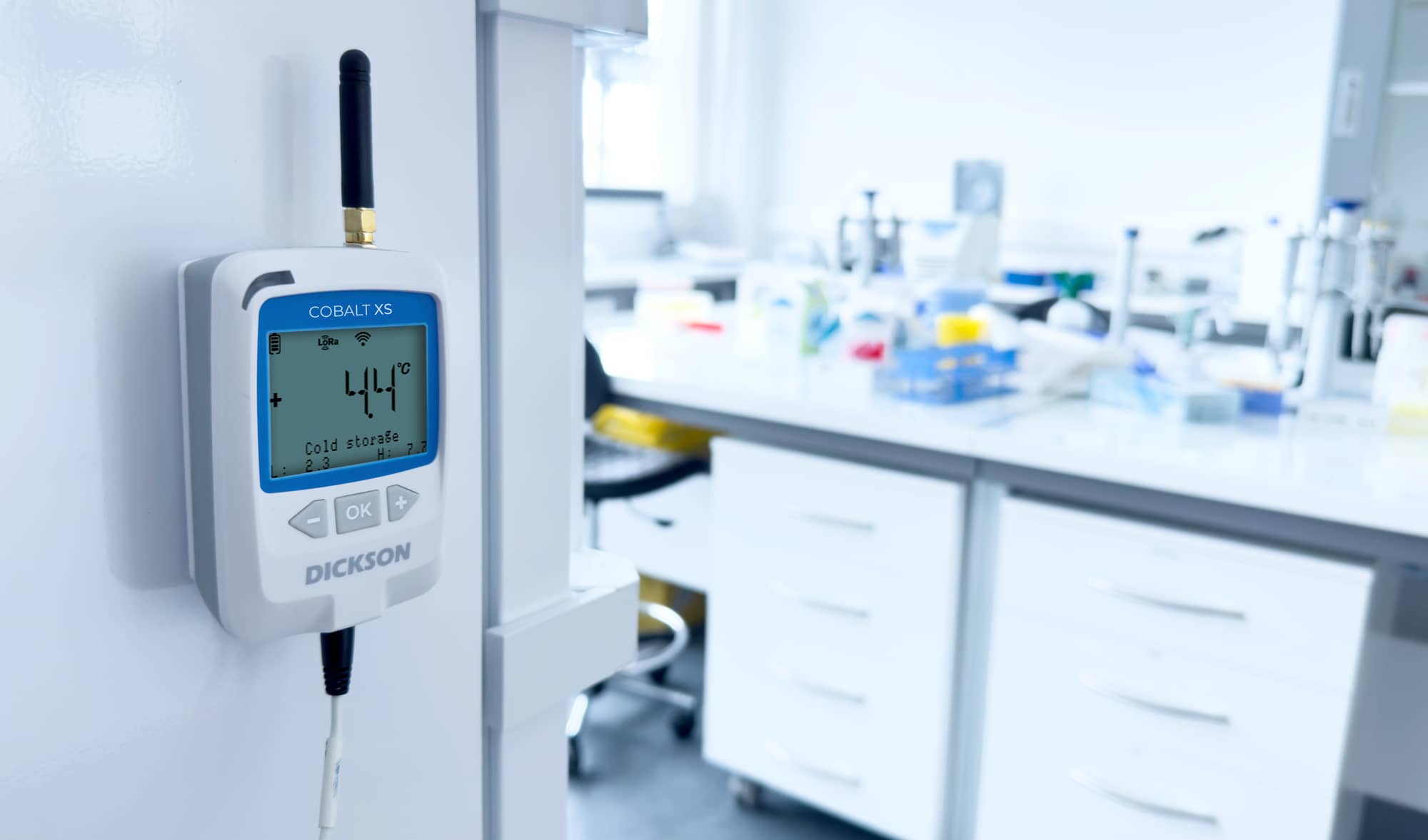
Monitoreo de la temperatura
Las soluciones de Dickson permiten el mapeo y monitoreo de temperatura en tiempo real en áreas sensibles como cámaras frigoríficas, almacenes farmacéuticos, incubadores de laboratorio, salas limpias y refrigeradores de laboratorio. Estos sistemas de monitoreo son esenciales para garantizar que los productos sensibles a la temperatura (vacunas, muestras biológicas, medicamentos inyectables, etc.) permanezcan en condiciones que cumplan con los estudios de estabilidad. Con tecnología de punta, los registradores de datos Dickson pueden recopilar, registrar y transmitir datos precisos durante períodos prolongados, lo que reduce los riesgos asociados con las variaciones de temperatura.
Monitoreo de la humedad
Los registradores Dickson pueden incluir sondas y sensores de humedad, otro parámetro crítico para productos sensibles. Nuestros sistemas de monitoreo y soluciones de mapeo garantizan que las condiciones de humedad cumplan con los requisitos de almacenamiento y producción establecidos por las GMP, minimizando el riesgo de degradación del producto.
CO2 y otros parámetros
Para entornos de producción o laboratorio que requieren un control estricto de CO2, como los incubadores de laboratorio de cultivos celulares, las soluciones de monitoreo de Dickson integran sensores de alta precisión que garantizan el cumplimiento de las normas GLP y GMP. La flexibilidad de los sistemas de monitoreo de Dickson permite la personalización de acuerdo con los requisitos específicos de cada laboratorio o centro de producción.

Gestión de desviaciones con los sistemas de monitoreo de Dickson
Uno de los principales retos de las empresas farmacéuticas es la gestión de las desviaciones de temperatura, humedad o CO2. Los sistemas de monitoreo en tiempo real de Dickson están diseñados para detectar rápidamente cualquier desviación y activar alertas automáticas, lo que permite que el personal responsable intervenga antes de que el producto se vea comprometido.
Alertas en tiempo real:
Los sistemas Dickson están equipados con mecanismos de alerta que notifican inmediatamente a los equipos cuando las condiciones ambientales superan los rangos predefinidos. Las alertas se pueden configurar para activar alarmas visuales y sonoras o enviar notificaciones por SMS o correo electrónico, lo que garantiza respuestas rápidas y eficaces para evitar la pérdida de productos.
Documentación de cumplimiento y trazabilidad con la experiencia de Dickson
La documentación precisa y conforme a la normativa de las medidas correctoras y de seguimiento ambiental es esencial en virtud de GxP. Dickson ha desarrollado soluciones de software avanzadas, DicksonOne y OCEAView, que centralizan la recopilación y el procesamiento de datos ambientales, simplificando la trazabilidad y la gestión de auditorías.

¿Desea más Información?
Hable con un especialista sobre el monitoreo continuo de temperatura, humedad y de otros parámetros físicos
Nuestro equipo de profesionales está listo para ayudarlo a encontrar la solución perfecta para el monitoreo continuo.
Envíenos un mensaje o llámenos al +33 (0) 4 99 13 67 30.






